G.D. Kotzalidis, A. Facchi, L. Tarsitani, P. Pancheri - Vol. 8, June 2002, Issue 2
Testo Immagini Bibliografia Summary Indice
Effetti della somministrazione di
antipsicotici sullespressione regionale
cerebrale di geni immediati precoci (IEG)
Effects of the administration of antipsychotic
drugs on the regional brain expression
of immediate early genes (IEGs)
Fig. 1. Laloperidolo, la raclopride e la clozapina aumentano il c-fos attraverso linibizione di recettori della famiglia dei D2, mentre la D-amfetamina e il CY 208-243 lo aumentano attraverso la stimolazione di recettori della famiglia dei D1 (basata su dati di Robertson e Jian, 1995(101)) Haloperidol, raclopride and clozapine increase c-fos through D2-like receptor blockade, whereas D-amphetamine and CY 208-243 increase it through the stimulation of D1like receptors (based on data from Robertson and Jian, 1995(101)).
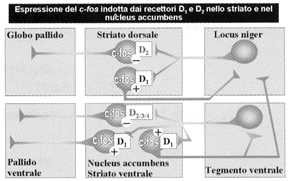
Fig. 2. Interazione tra famiglie recettoriali dopaminergiche nel controllo dellespressione di c-fos nello striato di ratto. Per semplicità, viene riportata lazione dellaloperidolo solo sui recettori D2, sui quali la potenza inibitrice del farmaco è più potente rispetto a quella che ha il farmaco stesso sui recettori D1 (basata su dati di Konradi e Heckers, 1995(103)) Interaction between dopamine receptor families in controlling the expression of c-fos in rat striatum. For the sake of clarity, haloperidol action on only D2 receptors is reported; this drug blocks these receptors more potently than those of the D1 family (based on data from Konradi and Heckers, 1995(103)).
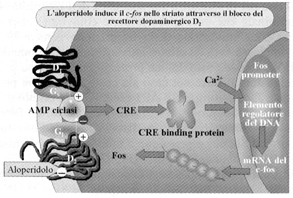
Fig. 3. Azione degli IEG nellindurre il sito AP-1 (dati basati su Doucet et al., 1996(41)) IEG action in inducing the AP-1 site (based on data from Doucet et al., 1996(41)).
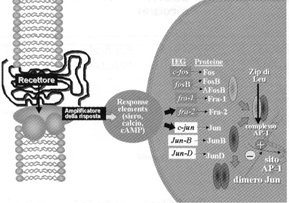
Fig. 4. Autoradiografie su campo chiaro: induzione di cellule positive al Fos (colorazione più chiara) e ibridizzazione in situ con sonde radiomarcate con (35)S dellmRNA di peptidi oppioidi (granuli scuri) (encefalina-1a e 3a riga e dinorfina-2a e 4a riga) da parte della clozapina (antipsicotico atipico) e dellaloperidolo (neurolettico classico) nello striato, nellisola maggiore del Calleja, nel nucleus accumbens e nel nucleo settale laterale del ratto (da Guo, 1998(68)) Bright field autoradiography: induction of Fos-positive cells (more lightly stained) and in situ hybridisation with (35)S mRNA radiolabelled probes for opioid peptides (dark granules) (enkephalin-1st and 3rd row and dynorphin-2nd and 4th row) on behalf of clozapine (atypical antipsychotic) and haloperidol (classical neuroleptic) in the rat striatum, major island of Calleja, nucleus accumbens, lateral septal nucleus (from Guo, 1998(68)).
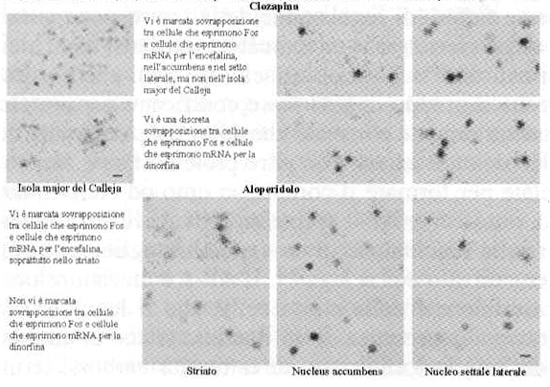
Fig. 5. Interazioni tra sistema glutamatergico, adenosinergico e dopaminergico nellinduzione di c-fos nei gangli basali di ratto; gli effetti dei recettori A2A sono fasici, quelli dei recettori A1 sono tonici. La stimolazione dei recettori NMDA e A2A induce una riduzione di affinità dei recettori D2; vengono evidenziati due neuroni che espongono recettori D2 sui loro dendriti, uno che espone anche recettori NMDA ed uno che espone anche recettori adenosinici A2A; tuttavia, è possibile che tutti e tre i sottotipi recettoriali coesistano nello stesso neurone (basata su dati di Boegman e Vincent, 1996(108); Harvey e Lacey, 1997(109); Ferré et al., 1999(110); Golembiowska e Zylewska, 1997(111); Salim et al., 2000(112)) Interactions between glutamatergic, adenosinergic and dopaminergic systems in inducing c-fos in rat basal ganglia; Adenosine A2A receptor effects are phasic, those of the A1 receptors are tonic. NMDA and A2A receptor stimulation induces a reduction in the affinity of D2 receptors; two neurones are shown that exhibit D2 receptors on their dendrites, one exhibiting also NMDA receptors and one exhibiting also A2A adenosine receptors; however, it is possible that all three receptor subtypes co-exist in the same neurone (based on data from Boegman and Vincent, 1996(108); Harvey and Lacey, 1997(109); Ferré et al., 1999(110); Golembiowska and Zylewska, 1997(111); Salim et al., 2000(112)).
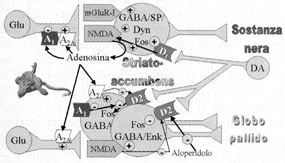
Fig. 6. Fotomicrografie in campo oscuro dello striato mediale con colorazione retrograda al fluoro-oro che visualizza i neuroni strionigrali GABA/Sostanza P/Dinorfinergici (diametro di circa 18 mm; alla punta dei triangoli) dopo lesione con 6-idrossidopamina del tratto dopaminergico nigro-striatale (a sinistra); la marcatura corrisponde grosso modo alle cellule DFosB-positive. Al centro vengono evidenziati i nuclei di neuroni DFosB-immunoreattivi (punte di triangoli) dopo trattamento cronico con lagonista D1 CY 208-243. Viene evidenziata una marcatura più accentuata che corrisponde grosso modo alle cellule GABA/Sostanza P/Dinorfinergiche. A destra vengono evidenziati i neuroni GABA/Sostanza P/Dinorfinergici strionigrali dopo lesione con 6-idrossidopamina del tratto dopaminergico nigrostriatale omolaterale e trattamento cronico con lagonista D1 CY 208-243; la marcatura, non evidente in questa sezione striatale, si limita alla substantia nigra, pars reticulata (non mostrata), senza corripondere alle cellule DFosB-positive. In basso, nuclei di neuroni DFosB-immunoreattivi nello striato mediale del ratto dopo lesione con 6-idrossidopamina del tratto dopaminergico nigrostriatale e trattamento cronico con lagonista D1 CY 208-243; laccentuazione dellimmunoreattività non corrisponde esattamente alle cellule GABA/Sostanza P/dinorfinergiche (confronta immagini in alto a sinistra e al centro) (da Doucet et al., 1996(14)) Dark-field photomicrographs of medial striatum with fluorogold retrograde staining showing strionigral GABA/Substance P/Dynorphinergic neurones (about 18 mm diameter; arrowheads) after 6-hydroxydopamine lesion of the nigro-striatal dopaminergic pathway (at left); labelling roughly corresponds to DFosB-positive cells. Nuclei of DFosB-immunoreactive neurones are shown in the middle (arrowheads) after chronic treatment with the D1-agonist, CY 208-243. Enhanced labelling is shown, grossly corresponding to GABA/Substance P/Dynorphinergic cells. Strionigral GABA/Substance P/Dynorphinergic neurones after 6-hydroxydopamine lesion of the ipsilateral nigrostriatal dopaminergic tract and chronic treatment with the D1 agonist, CY 208-243, are shown on the right; labelling, not evident in this striatal cut, is limited to substantia nigra, pars reticulata (not shown), without corresponding to DFosB-positive cells. At the bottom, nuclei of DFosB-immunoreactive neurones in rat medial striatum after 6-hydroxydopamine nigrostriatal dopaminergic tract lesion and chronic treatment with the D1 agonist, CY 208-243; immunoreactivity enhancement does not exactly correspond to GABA/Substance P/dynorphinergic cells (compare images at left top and in the middle) (from Doucet et al., 1996(14)).
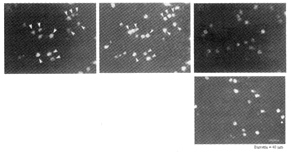
Fig. 7. Controllo frontocorticale dellespressione di c-fos. A sinistra, una fotomigrografia (immunoistochimica con anticorpo di coniglio anti-GAD67 e metodo di perossidasi-antiperossidasi con diaminobenzidina come cromogeno [scuro]; anticorpo anti-Fos di montone e tecnica di immunoperossidasi con avidina/biotina e diaminobenzidina più cloruro di cobalto e solfato di ammonio [nero]) di nuclei con immunoreattività Fos-simile nella corteccia prefrontale del ratto dopo stimolazione con un agonista dei recettori 5-HT2A/2C.(1-(2,5-dimetossi-4-iodofenil-2-aminopropano [DOI]) (in nero) in interneuroni GABAergici GAD67-positivi (frecce) e in neuroni piramidali GAD67-negativi [presumibilmente glutamatergici] (punta di freccia). Vi sono anche neuroni GABAergici GAD67-positivi (nuclei colorati in scuro) che non esprimono immunoreattività Fos-simile dopo stimolazione 5-HT2A/2C (barretta=10 mm) (da Abi-Saab et al. (361)). Sopra è raffigurato un modello circuitale che tenta di spiegare i dati della fotomicrografia, includendo anche altri dati della letteratura (Harvey e Lacey (109); Svensson et al. (363)) Control of c-fos expression in the frontal cortex. At left, photomigrograph (immunohistochemistry with anti-GAD67 rabbit antibody and peroxidase-antiperoxidase method with diaminobenzidine as a chromogene [dark]; sheep anti-Fos antibody and avidine/biotine immunoperoxidase technique and diaminobenzidine plus cobalt chloride and ammonium sulfate [black]) of Fos-like immunoreactive nuclei in rat prefrontal cortex after stimulation with a 5-HT2A/2C receptor agonist (1-(2,5-dimetossi-4-iodofenil-2-aminopropano [DOI]) (in black) in GAD67-positive GABAergic interneurones (arrows) and GAD67-negative pyramidal neurones [presumably glutamatergic] (arrowhead). There are also GAD67-positive GABAergic neurones (nuclei staining dark) that do not express Fos-like immunoreactivity after 5-HT2A/2C stimulation (bar=10 mm) (from Abi-Saab et al. (361)). On the top, a circuit model is shown that provides an explanation for data stemming from the photomicrograph, including other data from literature as well (Harvey and Lacey (109); Svensson et al. (363)).
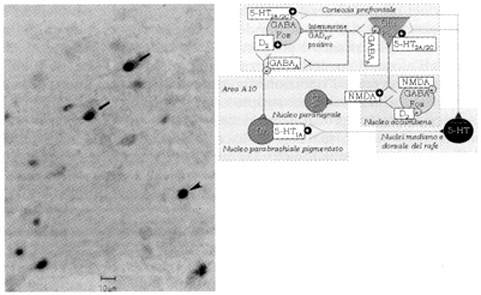
Fig. 8. Aumentato Wnt-1 nellarea CA4 dellippocampo di un paziente schizofrenico. Sezioni deparaffinizzati di cervello umano trattate con alcol contenente perossido di idrogeno (H2O2), sono state esposte a siero di coniglio al 10% e successivamente incubate con anticorpo anti-Wnt-1 di capra diluito all1:1000 per 24 h a 4°C in camera umidificata, poi lavate in PBS ed incubate per 1 h con IgG di coniglio anti-capra biotinilata, rilavata con PBS ed incubata per 1 ora con streptavidina perossidasi-coniugata. Colorate con 40 mg/mL di dimetilaminoazobenzene e 0,002% H2O2. Lelaborazione immunoistochimica è stata effettuata contemporaneamente per tutti e 20 i soggetti (10 schizofrenici e 10 soggetti di controllo appaiaiti per età e sesso) su sezioni colorata con colorazione di Nissl. Per ogni cinque sezioni effettuate per soggetto, una è stata controllata con colorazione allematossilina-eosina per stabilire le coordinate neuroanatomiche e per la conta delle cellule nucleolate; i margini delle aree CA1, 2, 3 e 4 sono stati delineati attraverso i criteri di de Lorente (de Lorente R. Studies on the structure of cerebral cortex. II. Continuation of the study of the ammonic system. Journal of Psychology and Neurology, 1937; 46: 113-177) (da Miyaoka et al., 1999(389)) Increased Wnt-1 levels in the CA4 hippocampal area of a schizophrenic patient. Deparaffinised sections of human brain treated with alcohol contining hydrogen peroxide (H2O2), were exposed to rabbit 10% serum and thereafter incubated with 1:1000 diluted goat anti-Wnt-1 antibody for 24 h at 4°C in a humidified room, than washed in PBS and incubated for 1 h with biotinylated anti-goat rabbit IgG, washed again with PBS and incubated for 1 hour with peroxidase-conjugated streptavidine. Stained with 40 mg/mL dimethylaminoazobenzene and 0.002% H2O2. Immunohistochemical processing was carried-out concomitantly for all 20 subjects (10 schizophrenic patients and 10 age- and sex-matched controls) on Nissl-stained sections. For every five section per subject, one was controlled through haematoxyline-eosine staining to establish neuroanatomic co-ordinates and nucleolated cell count; CA1, 2, 3 e 4 area boundaries were outlined through the de Lorente criteria (de Lorente R. Studies on the structure of cerebral cortex. II. Continuation of the study of the ammonic system. Journal of Psychology and Neurology, 1937; 46: 113-177) (from Miyaoka et al., 1999(389)).
Fig. 9. Modello della molecola di axina di ratto con i diversi siti che legano vari substrati. Basato su dati di: Ikeda et al., 1998(392) Model of rat axin molecule with the various sites that bind different substrates. Based on data from Ikeda et al., 1998(392).
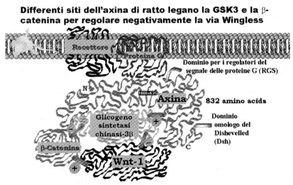
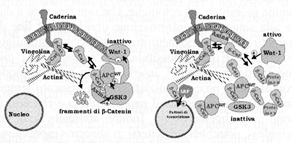
Fig.10. Regolazione del pool di b-Catenina da parte della GSK3b e del Wnt-1. In condizioni di alta attività GSK3b/bassa attività Wnt-1 (a sinistra), vi è aumentato catabolismo della b-catenina e di conseguenza, i livelli di questultima sono tenuti sotto controllo. In condizioni di bassa attività GSK3b/alta attività Wnt-1 (a destra), si raggiungono alti livelli a riposo di b-catenina e viene facilitata la formazione di complessi con varie proteine; APCWT: tumour suppressing protein, wild type; GSK3: glicogeno sintetasi chinasi 3-b ZW3 omologa, inattiva; LEF-1: Lymphoid Enhancer Factor-1 (modificato da Papkoff et al. (393); integra dati di Sakanaka et al. (395)) GSK3b and Wnt-1 regulation of b-Catenin pool. Under high GSK3b/low Wnt-1 activity conditions (left), there is increased b-catenin metabolic breakdown, hence, the levels of the latter under control. Inder low GSK3b/high Wnt-1 activity conditions (right), high resting b-catenin levels are reached and consequently, the formation of complexes with various proteins is facilitated; APCWT: tumour suppressing protein, wild type; GSK3: 3-b ZW3 homologous glycogen synthase kinase, inactive; LEF-1: Lymphoid Enhancer Factor-1 (modified from Papkoff et al. (393); integrates data from Sakanaka et al. (395)).